En 2021, la France a engagé une expérimentation médicale sur le cannabis thérapeutique. Tous les feux sont au vert, mais les autorités vont-elles oser sauter le pas ?
« On a déjà vu des expérimentations ne jamais aboutir. » Le professeur Nicolas Authier, président du comité scientifique sur le cannabis médical, craint que l’expérimentation en cours ne soit jamais généralisée en France.
Depuis mars 2021, 2600 patients ont été inclus pour suivre un traitement à base de cannabis. Cette généralisation, si elle voyait le jour, pourrait concerner entre 100 000 et 300 000 patients en France. Pour cela, il faudrait que le Parlement français et les autorités de santé osent franchir le Rubicon. Le sentier est escarpé puisque la plante de cannabis est un stupéfiant et que le sujet polémique est hautement inflammable.
L’hypothèse d’une généralisation prochaine est venue de la Direction générale de la santé (DGS).
En avril 2023, elle a émis l’idée d’une entrée dans le droit commun de ces médicaments à base de cannabis dès 2024. Pour Nicolas Authier, chef du service de pharmacologie médicale au CHU de Clermont-Ferrand, « c’est une bonne nouvelle, parce que pour l’instant, on n’avait pas beaucoup de signaux positifs ». En attendant, l’expérimentation a été prolongée d’un an, jusqu’en mars 2024.
« Pendant les deux premières années de l’expérimentation, la DGS n’a ni soutenu le dispositif, ni anticipé une généralisation. C’est pour cela qu’on est sur une année de prolongation. En revanche, il semblerait qu’elle ait pris le sujet à bras-le-corps depuis le début de l’année. Un calendrier sur la sortie de l’expérimentation a été diffusé », résume Aurélien Bernard, spécialiste des questions liées aux cannabis, fondateur du site newsweed.fr.
Cependant, le temps presse. Si d’autres patients veulent pouvoir profiter des principes actifs du cannabis en 2024, il va falloir que la généralisation soit discutée au Parlement avant la fin de l’année.
« Fin juin, début juillet au plus tard, il faut qu’on dispose de textes consolidés afin qu’ils puissent être intégrés au futur Projet de loi de financement de la Sécurité sociale (PLFSS), qui sera discuté en octobre. Si ces textes ne sont pas intégrés dans le PLFSS voté avant la fin de l’année, alors on sera coincé et on sait qu’il ne se passera rien en 2024. On risquerait de partir sur une quatrième année d’expérimentation », alerte le professeur Nicolas Authier.
Le délai est très court et à part des paroles, le président du comité scientifique n’a aucune garantie tangible. Nous avons interrogé la DGS pour savoir si une application dans le droit commun était prévue pour 2024. Sans le dire explicitement, elle semble intégrer cette hypothèse : « Les prochains travaux porteront sur la définition des contours de la période intermédiaire à prévoir jusqu’à la mise en œuvre effective du dispositif, du parcours patient, ainsi que de la procédure d’autorisation des acteurs et des produits. »
Une expérimentation commencée en 2021
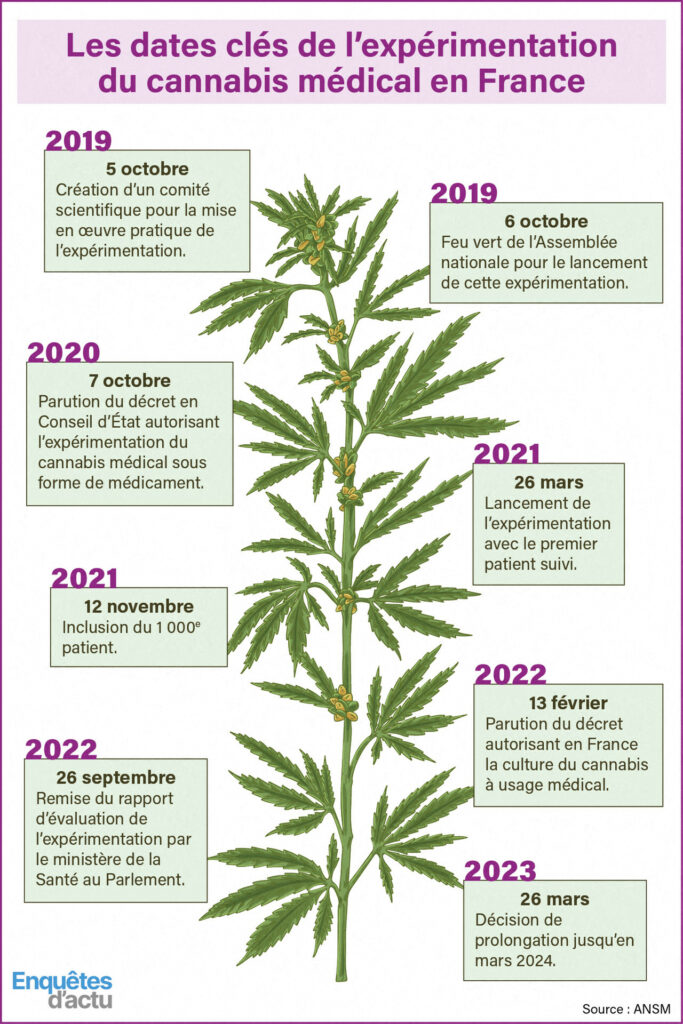
En France, une réflexion sur l’usage du cannabis dans un cadre médical est engagée depuis 2018. Un comité scientifique temporaire a été mis en place et s’est très vite positionné en faveur de l’utilisation de ces nouveaux médicaments. C’est donc l’Agence nationale de sécurité du médicament (ANSM) qui a lancé cette expérimentation en 2021.
Par rapport au reste du monde, la France est à la traîne. Le cannabis médical est prescrit dans 38 États des États-Unis, avec une réflexion amorcée depuis les années 1990. En 1999, le Canada s’est lancé dans cette voie. Le cannabis thérapeutique est légal en Israël depuis 2001, depuis 2003 aux Pays-Bas. La Suisse a légiféré en 2011, la République Tchèque en 2013, l’Australie en 2016 et l’Allemagne s’est positionnée en faveur de ce traitement en janvier 2017.
Toutefois, la délivrance des médicaments à base de cannabis est extraordinairement contrôlée. Chaque pays signataire doit respecter les traités internationaux de contrôle des drogues et en référer à l’Organe international de contrôle des stupéfiants (OICS).
Depuis 2021, ce sont donc 2600 patients qui ont intégré le programme de l’ANSM en France. Certains en sont sortis et 1650 patients étaient encore suivis par les structures hospitalières volontaires en mai 2023. Au total, 1722 professionnels de santé ont été formés.
L’expérimentation ne concerne que cinq indications thérapeutiques :
- douleurs neuropathiques réfractaires (c’est-à-dire résistantes aux médicaments)
- effets indirects de la chimiothérapie comme les nausées et la perte d’appétit
- épilepsie réfractaire
- soins palliatifs
- sclérose en plaque.
« On n’est pas plus bête qu’un autre pays »
« Cette expérimentation est particulière, car ce n’est pas une étude de recherche classique sur l’efficacité du produit. Cette étude vise plutôt à tester la faisabilité de ce traitement en termes de fabrication, de transport, de prescription par le médecin, de délivrance par la pharmacie, de sécurité en termes d’effets indésirables ou de dépendance, ou encore de relais en ville », détaille Emmanuelle Kuhn, médecin de la douleur au sein du CHU de Nantes et présidente du Comité de lutte contre la douleur.
« L’expérimentation nous permet de voir qu’on va y arriver, on n’est pas plus bête qu’un autre pays, se réjouit le professeur Nicolas Authier. Ce sont des patients qui ont des pathologies sévères, douloureuses, ils comprendraient difficilement qu’on leur dise que c’est fini. Politiquement, ça serait délicat d’arrêter. »
Selon le président du comité scientifique, « une quatrième année d’expérimentation n’apporterait rien, si ce n’est une embolisation des structures hospitalières, parce qu’on a du mal à inclure de nouveaux patients vu qu’on n’arrive pas à passer le relais auprès de nos collègues médecins généralistes ».
C’est le principal point noir de cette expérimentation : la faible implication des médecins de ville. Seuls 139 sont engagés dans l’expérience. Pour eux, les lourdeurs administratives semblent trop importantes.
On leur demande de remplir un registre pour chaque patient. Ils doivent suivre une formation. Les contraintes intrinsèques à l’expérimentation ont freiné le relais avec les médecins généralistes. Mais si cette contrainte saute, ça fera comme pour tous les médicaments : si on prescrit un médicament qui fonctionne à l’hôpital, le médecin traitant reprendra la main.
Pour Karine Pansiot, pharmacienne membre du comité scientifique, « il est nécessaire en effet de développer le relais en ville » pour une « meilleure équité d’accès aux traitements ». Elle forme le vœu que « cette année supplémentaire permettra […] l’adhésion de nouveaux prescripteurs, en particulier des médecins généralistes ».
(©Enquêtes d’actu)
« Ça peut changer la vie, y compris des enfants »
Certains médicaments sont riches en CBD, d’autres en THC, et pour une troisième catégorie de produits, il s’agit d’un mélange des deux. Ces médicaments sont des huiles se consommant par voie orale.
Les cannabinoïdes
Le cannabis contient de très nombreux composants (près de 500) ; les cannabinoïdes représentant la principale classe. Les principaux cannabinoïdes sont :
– le tétrahydrocannabinol (THC) : classé parmi les substances hallucinogènes, il est responsable des effets psychoactifs stupéfiants et d’une partie des activités thérapeutiques de la plante.
– le cannabidiol (CBD) : il est psychoactif mais il n’induit pas les effets psychodysleptiques du THC. Il présente également un intérêt thérapeutique.
(Source : ministère de la Santé)
« Ces traitements ne permettent pas de guérir, mais d’apaiser notamment certaines douleurs », indique le professeur Nicolas Authier.
« Les doses efficaces sont obtenues en moyenne dès les trois premiers mois de l’expérimentation. On note une amélioration ressentie de leur état de douleur, qualifiée d’importante à très importante pour environ 40% des patients, incluant leur capacité à effectuer des activités, à bien dormir… », résume Emmanuelle Kuhn, médecin de la douleur.
Ces traitements s’adressent à des patients dont les médicaments ne fonctionnent pas ou plus. « On a des patients qui ont vu diminuer la fréquence de leur épilepsie alors qu’ils faisaient des crises tous les jours », explique le professeur Authier qui a vu ces médicaments « changer la vie » de patients, « y compris d’enfants ».
Pour le docteur Kuhn, du CHU de Nantes, il est évident qu’« il faut poursuivre », même si ce « nouveau traitement n’est pas dénué d’effets indésirables comme des troubles de la concentration, de la somnolence, des diarrhées… »
Un avis partagé par la pharmacienne et membre du comité scientifique, Karine Pansiot puisque « la majorité des [patients interrogés] ont vu leur qualité de vie améliorée. Il m’apparaît alors indispensable de pouvoir continuer à leur fournir des médicaments sécurisés […] ».
Des fournisseurs étrangers
Dans le cadre de l’expérimentation française, les médicaments étaient jusque-là fournis gracieusement par des entreprises étrangères : États-Unis, Israël, Canada… L’Assurance maladie n’a donc rien déboursé depuis 2021.
Avec la prolongation de l’expérimentation, ces dernières ont demandé une rétribution. L’ANSM n’est plus responsable de la sélection des fournisseurs, « c’est la DGS qui est désormais l’autorité compétente en la matière via des marchés publics. Les médicaments utilisés ne seront donc plus fournis à titre gratuit par les entreprises participantes », prévient Karine Pansiot du comité scientifique.
Mais ils ne proviendront toujours pas d’entreprises françaises, qui sont totalement hors course pour le moment. Seulement cinq ont obtenu des licences de recherche sur le cannabis médical. « Elles peuvent faire pousser du cannabis, mais elles sont obligées de détruire les récoltes une fois les fleurs récupérées », précise Aurélien Bernard de newsweed.
La biotech Overseed a été la première du pays à obtenir l’autorisation délivrée par l’ANSM de développer la recherche et le développement sur la plante et la conception de médicaments. « Il m’a paru intéressant de positionner un projet ambitieux, en avance de phase par rapport à la réglementation », confie à Enquêtes d’actu Hugues Péribère, le fondateur de la start-up.
Cet ingénieur agronome de formation espère pouvoir vendre ses produits dès que le DGS lui aura donné accès au marché. « Ce sera a priori pour le premier semestre 2024, puisque le calendrier de la DGS est connu. Espérons qu’il soit tenu », escompte Hugues Péribère.
Vers la création d’une filière française ?
Dans cette perspective, nombreux sont ceux qui souhaitent voir naître une filière française de production, aujourd’hui inexistante. « Il faudra entre deux et trois ans », selon le professeur Nicolas Authier.
Cela prend du temps de produire du cannabis médical, « parce que cette plante hybridée par des gens talentueux l’a été pour le marché récréatif [consommation pour le plaisir, NDLR], mais pas dans un objectif agronomique ou médical. Il faut faire ce travail agronomique pour stabiliser des variétés […]. Pour produire un médicament de qualité médicale, il faut le faire en démontrant qu’on peut apporter une répétabilité et une fiabilité dans les opérations menées », explique Hugues Péribère.
L’émergence de cette filière nationale est « un des objectifs de l’ANSM », affirme le docteur Emmanuelle Kuhn médecin au CHU de Nantes, afin de contrer de possibles difficultés d’approvisionnement. « Il existe un point de vigilance sur la sécurisation de la continuité du traitement, comme cela a été le cas pendant la crise du Covid avec d’autres traitements par exemple », poursuit Emmanuelle Kuhn.

Emmanuelle Kuhn, médecin de la douleur au sein du CHU de Nantes, participe à l’expérimentation sur l’usage du cannabis médical. (©Emmanuelle Kuhn)
Mais tant qu’il n’y aura pas de cadre réglementaire clairement identifiable, « les investisseurs seront frileux », prévient Aurélien Bernard de newsweed : « Lâcher 10 millions d’euros, alors qu’on ne sait pas s’il y aura un circuit de distribution, ça serait un peu cavalier. Le marché sera d’abord ouvert aux opérateurs étrangers, parce qu’ils ont l’expérience et les capitaux. »
Xavier Saiz, secrétaire du syndicat des professionnels du chanvre, regarde avec inquiétude les entreprises étrangères passer devant les structures françaises. Il doute que les producteurs français puissent avoir les reins assez solides pour respecter toutes les normes de sécurisation et de qualité.
Est-ce qu’ils vont avoir les moyens d’investir 1 ou 2 millions d’euros pour répondre à ces appels d’offres ? Ça va être compliqué. Les entreprises étrangères, avec l’avance qu’elles ont, sont déjà capées pour.
Il demande un « allégement des contraintes » pour permettre à davantage d’entreprises françaises de se lancer. Si c’était le cas, « il y aurait cinq entreprises au minimum qui pourraient fournir les produits avec un suivi de traçabilité. C’est assez frustrant. »
Xavier Saiz a mis au point trois logiciels (cannatracking) qui permettent de rendre transparentes et infalsifiables toutes les analyses, tout en garantissant une traçabilité complète du producteur au patient final.
Le secrétaire du syndicat professionnel du chanvre demande notamment l’obtention de licences THC temporaires.
Hugues Péribère reconnaît que « le nombre de contraintes est considérable », mais ce sont celles des produits stupéfiants. « Chaque feuille de plante est suivie, tracée. Quand vous détruisez une plante, elle doit être identifiée. […] On est sur des sites sécurisés, contrôlés, des établissements qui font l’objet de réglementations bien particulières gérées par l’Agence du médicament », rappelle Hugues Péribère, fondateur d’Overseed.
Vers une légalisation du cannabis ?
Si la France est à ce point en retard, c’est peut-être dû au fait qu’« il y a une confusion avec le cannabis récréatif dans la tête des décideurs politiques », involontaire ou entretenue, reconnaît le spécialiste Aurélien Bernard.
Le professeur Nicolas Authier est bien obligé de constater qu’« il y a quelques médecins et scientifiques qui n’échappent pas à des positions dogmatiques et ont du mal à prendre du recul ».
Sauf que le président du comité scientifique sur le cannabis thérapeutique est formel : « On n’est pas du tout en train de passer par la petite porte pour légaliser le cannabis en France. L’un ne fera pas le marchepied de l’autre. Est-ce que quand on a donné accès à la morphine, on a légalisé l’héroïne ? Est-ce que quand on a donné accès à la poudre d’opium, on a légalisé l’usage de l’opium ? Il n’y a aucun lien. »
Une enquête réalisée par Raphaël Tual et Farah Sadallah (actu Nantes)
Suivez toute l’actualité de vos villes et médias favoris en vous inscrivant à Mon Actu.
>>Lire aussi : Cannabis à usage médical : l’expérimentation prolongée d’un an








De quoi parle t on , des 200 m2 de chanvre cultivés a la timone a 0.3 % de THC ? Pour en plus en sortir des merdes synthétiques et hors de prix du style sativex . Arrêtez de nous les briser avec vos mensonges et règlementez l’autoproduction 1 m2 et 4 pieds outdoor par foyer les malades qui le souhaitent pourront produire leur traitement proprement et en même temps vous assècherez les points de deal qui posent tant de problèmes !